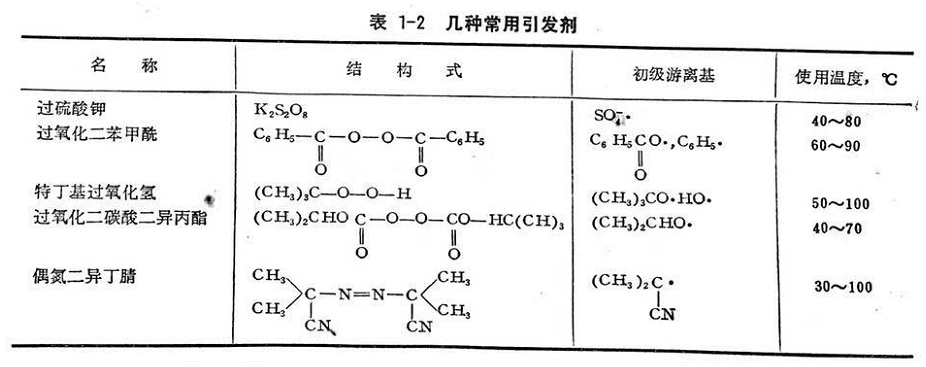
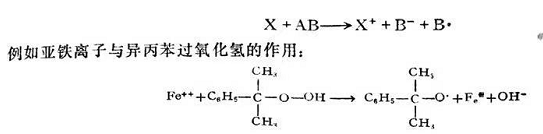
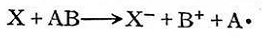過氧化氫引發劑的活化能為52千卡/克分子,而其相應的氧化還原體系H2O2-Ee"的活化能只有9,4千卡/克分子,異丙苯過氧化氫的活化能為30千卡/克分子,但其與亞鐵離子構成的氧化還原體系的活化能只有12千卡/克分子。
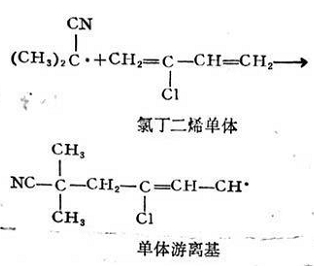
初級游離基尺·作用于單體分子時,激發雙鍵上的π電子,使之分離為兩個獨立電子,這是需要活化能的,R與其中一個獨立電子結合,放出一定的能量,而生成單體游離基RM。
在上述兩步反應中,引發劑的分解是吸熱反應,其分解活化能約為30千卡/克分子。而形成單體游離基的反應是放熱反應,活化能約為5~8千卡/克分子,反應極易進行,反應速度較快,即初級游離基R?一旦生成后,馬上就與單體M作用。故游離基RM的生長率主要決定于引發劑的分解速度。
在鏈的引發階段存在著許多副反應,主要是初級游離基或單體游離基與氧作用,或者是與雜質作用,這都將影響引發效率。要使鏈引發順利進行,就必須嚴格控制氧、雜質和阻聚劑,以盡量減少副反應。所謂阻聚劑就是一種捕提游離基的物質,它能極迅速與初級游離基作用,終止鏈反應。當聚合系統內有阻聚劑時,就產生誘導期,直到阻聚劑消耗完后,聚合作用才正常進行。通常,為防止純凈單體在生產或貯運中發生自然聚合現象,常在單體中加入少量阻聚劑(或叫穩定劑)。如加入0.05~0.1%的對苯二酚等。另一種阻滯劑或緩聚劑是只在反應初期阻滯聚合速度,使聚合速度減低,而不產生誘導期。引發效率就是引發劑分解產生的游離基數目,用于形成單體游離基的百分數,常用f%表示。通常,由于副反應的存在,以及單體性質、介質、引發劑濃度和反應溫度的影響,初級游離基的引發效率一般不能達到100%。用同一種引發劑去引發不同單體,引發效率也不同,見表1-3。

因為引發劑的分解速度直接關系到聚合速度,所以需知道引發劑的分解速度。由于引發劑是以端基形式參與聚合物的組成,加大引發劑用量,雖可以加快整個聚合速度,但卻使聚合物平均分子量降低。